我国创新药蓬勃发展,IND承办数连续三年增长
- 2021-10-13 14:00
- 作者:王宇恒
- 来源:
近年来,我国创新药研发增长态势喜人,临床试验申请IND承办数量连续三年增长,且增幅不断扩大,2021年前7月IND数量对比去年同期已翻倍增长,相比而言新药上市申请NDA整体变化幅度不大。
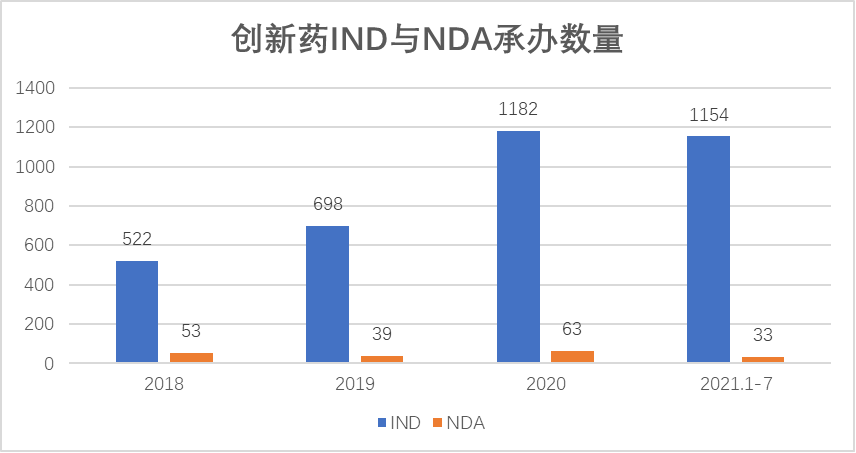
数据来源:Insight
如图所示,2018-2020年创新药IND承办数从522件增加至1182件;NDA整体变化趋势比较稳定,三年受理数分别为53件、39件及63件。2021年1-7月创新药(包括化药创新药、生物药创新药、中药创新药)IND受理数为1154件,同比大幅增长100%;NDA受理数为33件,略有下降。
其中,2021年1-7月化药1类创新药IND承办数为759件,NDA承办数21件。对比2020年同期,IND承办数大幅增长85%,NDA承办数增长17%。从以往趋势来看,2018-2020年化药IND承办数从372件增加至848件,CAGR为50%,总体临床承办数量增速喜人。NDA承办数量则较为稳定,平均每年承办数在20-40件之间,化药创新药仍保持着高昂的研发势头。
数据来源:Insight
2021年1-7月生物1类创新药的IND承办数为366件,NDA承办数为3件。对比2020年同期,IND承办数增加121%,NDA承办数降幅较大。从2018-2020年趋势来看,生物药1类创新药IND承办数从148件大幅增加至325件,2019年有小幅回落为136件,主要增幅在2020年。
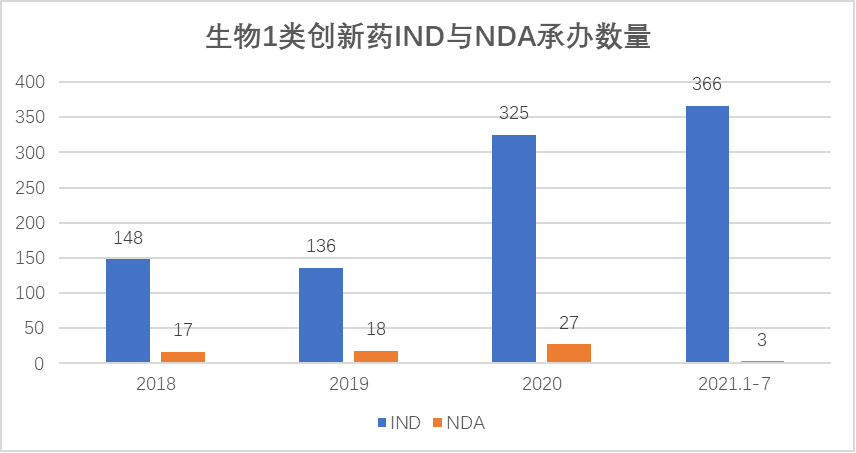
数据来源:Insight
2018-2020年,中药IND承办数从4件增加到9件,至2021年1-7月大幅增加至24件。2018-2020年NDA承办数量未有明显变化,其中2019年没有NDA承办。
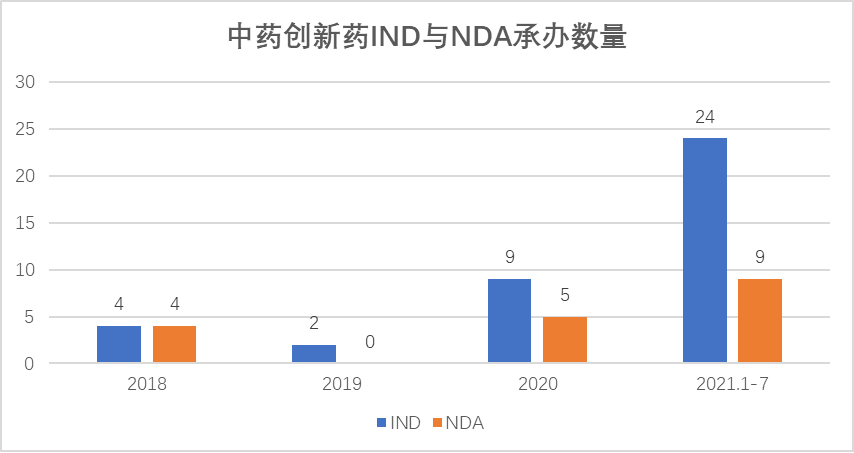
数据来源:Insight
根据Insight数据库,2018-2021年7月,对比同期化药1类创新药和生物创新药IND适应症分布可以发现,化药创新药增幅较大的适应症为肿瘤、内分泌以及免疫;生物创新药IND申请的主要适应症为肿瘤和免疫。生物创新药目前主要的IND受理类型为单抗类药物,从2018年的62件以60%的CAGR增加至2020年的159件;2021年1-7月单抗IND受理数为146件,同比去年增加66%。双抗的IND受理数更是明显增长,从2018年的5件增加至2020年的36件;今年更是有大幅增长,截至7月31日,双抗IND受理数已达到78件,超去年全年一倍以上。ADC和融合蛋白领域近两年IND受理数同样有明显增长,2020年分别达到13件及17件受理数;2021年前7月,ADC和融合蛋白领域IND受理数达到18件及23件,已超过2020年全年。
ADC方面,第一三共与阿斯利康共同开发的HER2 ADC药物DS-8201a国内目前已经在进行Ⅲ期临床试验。9月22日,荣昌生物的第四款ADC药物 RC118获批临床。8月27日,荣昌生物维迪西妥单抗的上市申请获受理,拟纳入优先审评审批。双抗方面,康方生物旗下的PD-1,VEGF靶点的双抗药物AK112有2项临床申请获受理,目前有针对卵巢癌、晚期/转移性实体瘤、晚期/转移性非小细胞肺癌、妇科肿瘤4种适应症的Ⅱ期临床试验正在进行中。康宁杰瑞旗下的CTLA4,PD-L1靶点的双抗药物KN046有2项临床申请获受理。艾伯维开发的CD20,CD3靶点的双抗药物Epcoritamab总计4例临床申请获受理。CAR-T方面,除了已经获批上市的复星凯特的阿基仑赛和药明巨诺的瑞基奥仑赛注射液,重庆精准生物针对BCMA,CD70双靶点的C-4-29的临床申请获受理,适应症为转移性肾细胞癌(RCC),实现了CAR-T治疗实体瘤的突破。药明巨诺第二款CAR-T疗法JWCAR129的IND申请也已获受理,该药物针对的靶点为BCMA,BCMA主要表达在多发性骨髓瘤(MM)细胞系及MM患者的细胞中。
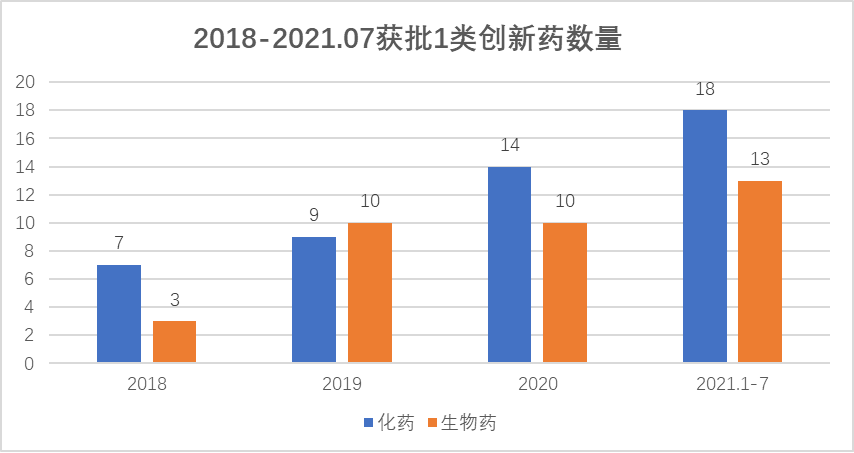
数据来源:Insight
如图所示,2018-2020年化药获批1类创新药数量由7例增加至14例,生物创新药获批数量从3例增加10例。2021年1-7月获批的1类创新药数量更是再创新高,获批数量为18例,生物药获批数量为13例。2021年7月共有3例新药获批,其中2种为进口药物,1种为1类新药。
1974年,加利福尼亚大学旧金山分校的J. Michael Bishop和博士后Harold Varmus意外发现正常细胞中也存在此前RSV病毒中发现的肿瘤基因src,证明肿瘤病毒早已存在正常基因组中。1982年,Weinberg等在人类膀胱癌细胞T24/EJ中发现了此前在逆转录病毒中发现的HRAS,使得RAS成为第一个被发现的人类原癌基因。KRAS蛋白是RAS蛋白家族中的重要一员,其具有“关闭”和“开启”两种状态。KRAS下游信号通路大多与细胞增殖、DNA合成、细胞迁移以及血管生成相关。当KRAS突变后,常会导致其下游的多条信号通路被激活,从而造成癌变。KRAS突变占据RAS家族突变总数的85%,并且其突变在众多癌症中均有表达,如果可以抑制KRAS蛋白的表达,就可以干扰其促进DNA合成、细胞增殖和血管生成的能力,因此多年来都是各大药企研发的重点领域。但其小分子抑制剂的开发却困难重重,被誉为“不可成药”的靶点。
安进公司Sotorasib(AMG510)的成功开发是KRAS抑制剂开发领域的重要标志性事件,Sotorasib针对124名KRASG12C突变的非小细胞肺癌患者的Ⅱ期临床试验结果表明,对于已经经过其他标准治疗的末线病人中,全部病人ORR为37.1%,其中经过一线治疗的病人ORR为39.6%,经过二线及以上治疗的病人ORR为35.2%,中位PFS为6.8个月。在中国,安进公司和百济神州已经达成合作,将共同进行Sotorasib在中国的开发工作;2021年2月,Sotorasib针对KRAS突变晚期/转移性非小细胞肺癌IND申请获批,已被国家药监局纳入拟突破性治疗药物品种。
表 国内KRAS抑制剂竞争格局
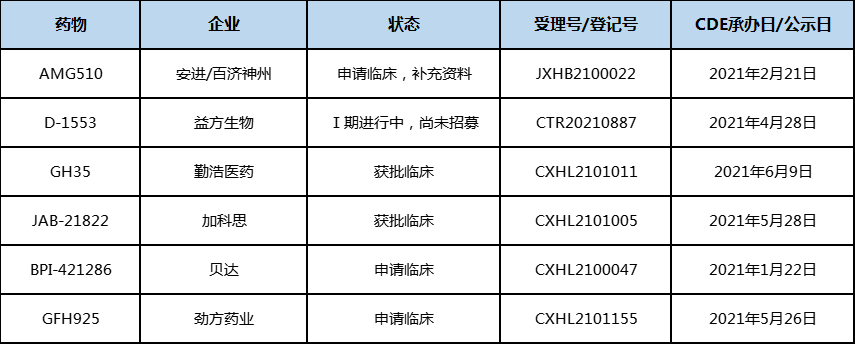
数据来源:CDE官网
2021年9月9日,璎黎药业的YL-15293治疗晚期恶性实体瘤获批临床试验,KRAS抑制剂正向着攻克实体瘤进军。
我国的创新药物尤其是生物创新药研发正在如火如荼发展中,可以预见未来将有更多的创新药物获批上市,战胜危急重症,为人民生命健康保驾护航。
《 》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐